F-dotierte, mit Kohlenstoff beschichtete Nano-Si-Anode mit hoher Kapazität: Vorbereitung durch gasförmige Fluorierung und Leistung für die Lithiumspeicherung
Autor:SU Nan, QIU Jieshan, WANG Zhiyu. F-dotierte, mit Kohlenstoff beschichtete Nano-Si-Anode mit hoher Kapazität: Vorbereitung durch gasförmige Fluorierung und Leistung für die Lithiumspeicherung. Journal of Inorganic Materials, 2023, 38(8): 947-953 DOI:10.15541/jim20230009
Abstrakt
Si anodes hold immense potential in developing high-energy Li-ion batteries. But fast failure due to huge volume change upon Li uptake impedes their application. This work reports a facile yet low-toxic gas fluorination way for yielding F-doped carbon-coated nano-Si anode materials. Coating of nano-Si with F-doped carbon containing high defects can effectively protect Si from huge volume change upon Li storage while facilitating Li+ transport and formation of stable LiF-rich solid electrolyte interphase (SEI). This anode exhibits high capacities of 1540-580 mAh·g-1 at various current rates of 0.2-5.0 A·g-1, while retaining >75 % Kapazität nach 200 Zyklen. Diese Methode befasst sich auch mit den Problemen hoher Kosten und Toxizität herkömmlicher Fluorierungstechniken, die Fluorquellen wie XeF2 und F2 verwenden.
Schlüsselwörter:Li-Ionen-Akku; Si-Anode; F-dotierter Kohlenstoff; Gasfluorierungsmethode
Die Entwicklung effizienter Technologien zur Energiespeicherung und -umwandlung wird dazu beitragen, das Ziel „CO2-Peaking und CO2-Neutralität“ zu erreichen. Lithium-Ionen-Batterien sind derzeit eine der am weitesten verbreiteten hocheffizienten Energiespeichertechnologien [1]. Allerdings verfügen kommerzielle Graphitanoden über eine geringe Lithiumspeicherkapazität, was die Energiedichte von Lithium-Ionen-Batterien stark einschränkt [2]. Silizium hat die Vorteile eines geringen Potenzials und reichlich vorhandener Reserven und seine theoretische spezifische Kapazität (4200 mAh·g-1) ist viel höher als die der Graphitanode, sodass es als mögliches Anodenmaterial für den Ersatz von Graphit angesehen wird [3 ]. Siliziummaterialien erreichen die Lithiumspeicherung auf der Grundlage der reversiblen Legierungsreaktion mit Lithiumionen. Dieser Prozess geht jedoch mit großen Volumenänderungen (~400 %) einher, was zu einer schnellen Pulverisierung und einem Ausfall der Elektrode führt und zu einem wesentlichen Engpass wird, der die praktische Anwendung von Lithium einschränkt Siliziumanoden [3- 4].
In den letzten Jahren haben Forscher verschiedene Strategien entwickelt, um die Stabilität und elektrochemische Leistung von Siliziumanoden zu verbessern. Zum Beispiel: Nanometerisierung [5], Strukturverbund mit leitfähigem Kohlenstoff und anderen Materialien [6-7] usw. Verbessern Sie die strukturelle Stabilität der Siliziumanode, indem Sie die mechanische Belastung verringern, die mit der Volumenausdehnung der Lithiumspeicherung im mikroskopischen Bereich verbunden ist Skala. Entwickeln Sie neue Elektrolyte oder Elektrolytzusätze, um die Stabilität und Coulomb-Effizienz der Festelektrolyt-Grenzflächenphase (SEI) auf der Oberfläche der Siliziumanode zu verbessern [8]. Entwickeln Sie effiziente Polymerbindemittel (wie Natriumcarboxymethylcellulose, Natriumalginat, Polyrotaxan auf Polyacrylsäurebasis [9] usw.). Stärken Sie die Bindungskraft zwischen aktiven Materialien, zwischen aktiven Materialien und leitfähigem Netzwerk sowie zwischen Elektrodenfilm und Stromkollektor [9-10]. Unter diesen ist die Kohlenstoffbeschichtung eines der wirksamsten Mittel, um die strukturelle Stabilität von Siliziumanoden zu verbessern und Oberflächen- und Grenzflächeneigenschaften zu modulieren [3-4,11]. Allerdings behindert die dicht beschichtete hochstabile Kohlenstoffschicht auch den Lithiumionentransport und schränkt die volle Leistung der Siliziumanode ein.
Darüber hinaus führen die wiederholten Volumenänderungen der Siliziumanode während des kontinuierlichen Lade- und Entladevorgangs auch dazu, dass der SEI-Film kontinuierlich bricht und immer wieder wächst, was zu einem kontinuierlichen Verlust von aktivem Lithium und Elektrolyt auf der Elektrodenoberfläche führt [12]. Als Reaktion auf die oben genannten Probleme schlägt diese Studie ein effizientes Gasphasenfluorierungsverfahren vor, um die Oberfläche des Siliziumanodenmaterials mit einer stark defekten amorphen Kohlenstoffschicht zu beschichten, die reich an Fluorelementen ist, um dessen Struktur und Grenzflächenstabilität zu verbessern. Verglichen mit der herkömmlichen Fluorierungstechnologie, die kostenintensive und hochtoxische Fluorquellen wie XeF2 oder F2 [13] verwendet, ist diese Strategie einfacher und weniger toxisch. Die mit Fluor dotierte Kohlenstoffschicht, die die Oberfläche von Nano-Siliziummaterialien bedeckt, kann die Volumenausdehnung von Lithium-eingebetteten Siliziumanoden wirksam abfedern und gleichzeitig die Transportfähigkeiten von Lithiumionen verbessern. Und ein hochstabiler SEI-Film, der reich an anorganischem Fluorid ist, wird vor Ort aufgebaut, um das Ziel zu erreichen, die Zyklenstabilität der Siliziumanode zu verbessern.
1 Experimentelle Methode
1.1 Materialvorbereitung
Herstellung von kohlenstoffbeschichtetem Nanosilizium (Si@C): 0,3 g kommerzielles Nanosiliziumpulver (Partikelgröße 20~100 nm, Aladdin's Reagenz) wurde mit Ultraschall in 28 ml eines gemischten Lösungsmittels aus entionisiertem Wasser und Ethanol (Volumenverhältnis 5:2) dispergiert. Nach Zugabe von 0,4 ml 3-Aminopropyltriethoxysilan 2 Stunden lang rühren, um eine gleichmäßige Dispersion A zu bilden. Lösen Sie 0,115 g 4,4-Dihydroxydiphenylsulfid und 0,1 g 3-Aminophenol in 28 ml eines gemischten Lösungsmittels aus entionisiertem Wasser und Ethanol (Volumenverhältnis 5:2), um eine homogene Lösung B zu bilden. Dispersion A und Lösung B gleichmäßig mischen, 0,1 ml Ammoniakwasser hinzufügen und rühren 30 Min., dann 0,14 ml Formaldehydlösung (37 % ~ 40 %) zugeben und unter ständigem Rühren bei 30 Grad 12 Stunden lang reagieren lassen. Nach der Reaktion wurde das mit Phenolharz beschichtete Nanosilica (Si@AF) durch dreimaliges Zentrifugieren und Waschen mit Ethanol und entionisiertem Wasser erhalten. Es wurde 3 Stunden lang bei 800 Grad in Argongas kalziniert, um kohlenstoffbeschichtetes Nanosilizium (Si@C) zu erhalten.
Herstellung von fluordotiertem, kohlenstoffbeschichtetem Nanosilizium (Si@CF): 100 mg Si@C und 200 mg Polyvinylidenfluorid (PVDF) wurden in einen argongeschützten Röhrenofen gegeben. Das Quarzschiffchen mit PVDF befindet sich stromaufwärts des Luftstroms und das Quarzschiffchen mit Si@C befindet sich stromabwärts des Luftstroms. Es wird 3 Stunden lang bei 600 Grad geröstet, um mit Fluor dotiertes, kohlenstoffbeschichtetes Nanosilizium (Si@CF) zu erhalten.
1.2 Batteriemontage und elektrochemische Leistungsprüfung
1.2.1 Batteriemontage
Bauen Sie die CR2016-Knopfbatterie zum Testen zusammen. Mischen Sie das Aktivmaterial, den leitfähigen Ruß und den Carboxymethylcellulose-Natrium-Binder gleichmäßig im Massenverhältnis 7:2:1. Als Lösungsmittel und Dispergiermittel wurde entionisiertes Wasser zugegeben und die erhaltene Aufschlämmung gleichmäßig auf die Kupferfolie als Arbeitselektrode aufgetragen. Die Beladung mit aktivem Material betrug 0,8~1,{{10}} mg·cm-2. Als Gegenelektroden und Referenzelektroden wurden Lithiummetallbleche verwendet. Der Elektrolyt ist eine DOL/DME-Lösung, gelöst in 1,0 mol/L LiTFSI (Lithiumbistrifluormethansulfonatimid) und 2,0 % LiNO3 (DOL ist 1, 3-Dioxolan, DME ist Ethylenglykol-Dimethylether, Volumenverhältnis 1:1). Montieren Sie die Zelle in einer mit Argon gefüllten Handschuhbox (Wassergehalt < 0,1 μL/L, Sauerstoffgehalt < 0,1 μL/L).
1.2.2 Batterieleistungstest
Verwenden Sie die elektrochemische Workstation IVIUM Vertex.C.EIS, um den Reaktionsmechanismus und die Reaktionskinetik der Batterie mithilfe der Cyclic Voltammetry (CV)-Methode zu analysieren. Der Spannungsbereich beträgt {{0}}.01~1,5 V und die Abtastrate beträgt 0.05~0.5 mV ·s- 1. Zur Analyse der Elektrodendynamik wurde die elektrochemische Impedanzspektroskopie (EIS) verwendet. Der Testfrequenzbereich betrug 100 kHz~10 mHz und die Störspannungsamplitude betrug 5,0 mV. Mit dem Batterietester Land CT2001A wurde die Lithiumspeicherleistung mithilfe der Konstantstrom-Lade- und Entlademethode untersucht. Das Spannungsfenster betrug 0,01–1,5 V (gegenüber Li/Li+) und die Stromdichte betrug 0,2–5,0 A·g-1.
2 Ergebnisse und Diskussion
2.1 Analyse von Aussehen, Struktur und Zusammensetzung von Materialien
Der Herstellungsprozess von mit Fluor dotierten, kohlenstoffbeschichteten Nano-Siliziummaterialien ist in Abbildung 1 dargestellt. Zunächst werden polymerbeschichtete Silizium-Nanopartikel (Si@AF) auf der Grundlage einer Phenol-Aldehyd-Kondensationspolymerisationsreaktion hergestellt und in amorphe, kohlenstoffbeschichtete Nanopartikel umgewandelt -Silizium-Nanopartikel (Si@C) bei hoher Temperatur. Anschließend wird Polyvinylidenfluorid als Fluorquelle verwendet und durch das Gasphasenfluorierungsverfahren bei hoher Temperatur Fluor in die Kohlenstoffschicht außerhalb der Siliziumnanopartikel dotiert. Abbildung 2(a) zeigt die XRD-Muster von Si@C- und Si@CF-Materialien. Beugungspeaks liegen bei 2θ=28 Grad, 47 Grad, 56 Grad, 69 Grad und 76 Grad. Sie entsprechen den Kristallebenen (111), (220), (311), (400) und (331) von einkristallinem Silizium (JCPDS 77-2108). Der breite Peak bei 2θ=25 Grad ~26 Grad wird der kurzreichweitig geordneten Kohlenstoffstruktur zugeschrieben, die durch die Carbonisierung des phenolischen Kondensationspolymerisationsprodukts entsteht. Die Kohlenstoffbeschichtungsschicht mit hoher Leitfähigkeit und ausgezeichneter struktureller Flexibilität kann den Pulverisierungsfehler von Siliziummaterialien während des Lade- und Entladevorgangs wirksam lindern und die Leitfähigkeit der Elektrode verbessern. Abbildung 2(b) ist das Raman-Spektrum von Si@C- und Si@CF-Materialien, wobei offensichtliche Absorptionspeaks bei 515, 947, 1350 und 1594 cm-1 auftreten. Darunter sind die Absorptionspeaks bei 515 und 947 cm-1 die charakteristischen Peaks von kristallinem Silizium, die aus der Photophononenstreuung erster Ordnung bzw. der transversalen Photophononenstreuung zweiter Ordnung von Silizium abgeleitet sind [14]. Die Absorptionspeaks bei 1350 und 1594 cm-1 entsprechen der Streckschwingung der aromatischen Kohlenstoffkonfiguration (G-Modus) bzw. der ungeordneten Defektkohlenstoffstruktur (D-Modus). Im Allgemeinen kann das Intensitätsverhältnis von D-Modus und G-Modus (ID/IG) verwendet werden, um den Grad der Defekte und Unordnung von Kohlenstoffmaterialien zu messen [15]. Im Vergleich zu Si@C-Material (ID/IG=0,99) erhöht sich das ID/IG von Si@CF-Material auf 1,08. Es zeigt, dass der Fluorierungsprozess die Defekte der Kohlenstoffbeschichtungsschicht erhöhen kann, was für eine dichte Beschichtung von Nanosilizium von Vorteil ist und gleichzeitig die Transportfähigkeiten von Lithiumionen verbessert.

Abb. 1 Schematische Darstellung der Herstellung von Si@CF

Abb. 2 (a) XRD-Muster, (b) Raman-Spektren, (c) XPS-Vermessungsscan, (d) hochauflösende F1s- und (e) Si2p-XPS-Spektren von Si@C und Si@CF, (f) TGA-Kurve von Si@CF
Das XPS-Vollspektrum zeigt, dass das Si@C-Material O-, N-, C- und Si-Elemente enthält (Abbildung 2(c)). Der atomare Anteil des F-Elements im Si@CF-Material, das nach der Fluorierungsbehandlung erhalten wird, beträgt etwa 1,8 %. Im hochauflösenden F1s-XPS-Spektrum (Abbildung 2(d)) entsprechen die beiden charakteristischen Peaks bei der Bindungsenergie von 686,3 und 687,8 eV CF bzw. Si-OF, wobei CF der dominierende ist. Es zeigt, dass die Fluorierungsbehandlung das Fluorelement erfolgreich in die amorphe Kohlenstoffschicht eingebracht hat, die auf der Oberfläche des Nanosiliziums aufgetragen ist. Die hochauflösenden XPS-Spektren von Si2p (Abbildung 2(e)) und F1s beweisen, dass Si-Atome chemisch mit dem F-Element in der Kohlenstoffschicht interagieren, indem sie Si-OF-Bindungen bilden, was für die dichte Beschichtung der Kohlenstoffschicht auf der Kohlenstoffschicht von Vorteil ist Silikonoberfläche. Die thermogravimetrische Analyse (TGA) zeigt, dass der Massenanteil von Si im Si@CF-Material etwa 85,17 % beträgt (Abbildung 2(f)).
Die SEM-Analyse zeigt, dass das Si@CF-Material aus Nanopartikeln mit einer Größe von besteht<100 nm (Figure 3(a~c)). After high-temperature carbonization and gas-phase fluorination treatment, the carbon material is still uniformly coated on the surface of the silicon nanoparticles.

Abb. 3 (ac) SEM-Bilder, (df) TEM-Bilder und (gi) Elementkartierung von Si@CF
Die TEM-Analyse zeigt, dass die Silizium-Nanopartikel vollständig und gleichmäßig von einer etwa zehn Nanometer dicken Kohlenstoffschicht umhüllt sind und eine Kern-Schale-Struktur bilden (Abbildung 3(d~e)). Silizium-Nanopartikel haben eine Einkristallstruktur, in der der Gitterabstand von 0.328 nm der (111)-Kristallebene von Si entspricht und die sie bedeckende fluordotierte Kohlenstoffschicht eine amorphe Struktur aufweist (Abbildung 3( F)). Das Elementverteilungsspektrum beweist, dass C- und Si-Elemente gleichmäßig in Si@CF verteilt sind (Abbildung 3(g~i)).
2.2 Elektrochemische Eigenschaften von Materialien
Abbildung 4(a, b) ist die CV-Kurve von Si@C- und Si@CF-Anodenmaterialien. Die Wobbelgeschwindigkeit beträgt 0,1 mV·s-1 und der Spannungsbereich beträgt 0,01~1,5 V. Im ersten Zyklus ist der schwache breite Peak in der Bereich von 0.1~0.4 V entspricht dem irreversiblen Prozess der Elektrolytzersetzung unter Bildung eines SEI-Films; Der Reduktionspeak bei 0.01 V entspricht dem Prozess, bei dem kristallines Silizium durch eine Legierungsreaktion eine Silizium-Lithium-Legierung (LixSi) bildet. Während des anschließenden Ladevorgangs entsprechen die beiden Oxidationspeaks bei 0.32 und 0.49 V dem Prozess der Entlegierung von LixSi unter Bildung von amorphem Silizium [16]. Durch die Fluorierungsbehandlung können strukturelle Dotierungs- und Ätzeffekte erzielt werden. In die auf der Oberfläche des Si-Materials aufgetragene amorphe Kohlenstoffschicht wird eine große Anzahl struktureller Defekte eingebracht, um einen dreidimensionalen Lithium-Ionen-Transportkanal zu bilden, den Lithium-Ionen-Transport zu beschleunigen und die elektrochemische Reaktivität des Si-Materials zu verbessern. Daher weist Si@CF bei 0,49 V einen schärferen Delithiierungsoxidationspeak auf als die Si@C-Anode ohne Fluordotierung. Während des anschließenden Entladevorgangs entspricht der neue Reduktionspeak bei 0,19 V dem Lithium-Insertionsprozess von amorphem Silizium, das während des ersten Ladevorgangs gebildet wurde [16-17]. Mit zunehmender Zyklenzahl ändern sich die Positionen des Oxidationspeaks und des Reduktionspeaks in der CV-Kurve nicht mehr, was darauf hindeutet, dass Si@C- und Si@CF-Anodenmaterialien nach dem ersten Laden und Entladen einem ähnlichen legierenden Lithiumspeichermechanismus folgen. Während dieses Prozesses nahmen der Oxidationspeak und der Reduktionspeak allmählich zu, was einen typischen Elektrodenaktivierungsprozess widerspiegelt.

Abb. 4 (a, b) CV-Kurven bei einer Abtastrate von 0,1 mV·s-1 und Lade-Entlade-Spannungskurven bei (c, d) 0,2 und (e, f) 0.4 A·g-1 für (a, c, e) Si@C- und (b, d, f) Si@CF-Anoden
Beim Lade- und Entladetest mit konstantem Strom wurde das Si-Anodenmaterial viermal bei einer niedrigeren Stromdichte (0,2 A·g-1) zyklisch aktiviert und anschließend auf seine Zyklenstabilität getestet eine Stromdichte von 0.4 A·g-1. Abbildung 4 (c, d) zeigt die galvanostatischen Lade- und Entladekurven von Si@C- und Si@CF-Anoden bei 0.2 A·g-1 und das Spannungsfenster ist 0 .01~1,5 V. Während des ersten Entladevorgangs bildeten beide eine lange Plattform im Spannungsbereich < {{20}},1 V, entsprechend dem Lithium-Insertionsprozess von kristallinem Silizium legieren. Dieser Prozess geht häufig mit einer niedrigen ersten Coulomb-Effizienz einher. Während des ersten Ladevorgangs wird die Silizium-Lithium-Legierung delithiiert und in amorphes Silizium mit einer geringeren Aktivierungsenergie für die Lithium-Insertion umgewandelt [18], wodurch das Lithium-Insertionspotential nach dem ersten Laden und Entladen auf 0,1–0,3 V ansteigt. Im Vergleich zu Si@C ist die spezifische Kapazität der ersten Entladung (2640 mAh·g-1) der Si@CF-Anode etwas niedriger. Allerdings ist die spezifische Kapazität der ersten Ladung (1739,6 mAh·g-1) höher und der erste Coulomb-Wirkungsgrad (65,9 %) ist etwa 45,8 % höher als der der Si@C-Anode. Die Lade-Entlade-Kurve des SEI-Bereichs der Si@CF-Negativelektrode ist kürzer als die von Si@C, was darauf hindeutet, dass sich auf der Oberfläche ein stabilerer SEI-Film bildet. Dies liegt daran, dass die mit Fluor dotierte Kohlenstoffschicht die Bildung eines SEI-Films begünstigt, der anorganische Komponenten (wie LiF) und eine höhere Stabilität auf der Oberfläche der Siliziumanode enthält, wodurch irreversibler Lithiumverlust und Elektrolytverbrauch reduziert werden [19].
Figure 4(e~f) shows the charge and discharge curves of Si@C and Si@C-F negative electrodes at a current density of 0.4 A·g-1 after activation. After 100 cycles, the Si@C-F anode can still maintain a high specific capacity of 1223 mAh·g-1, with a capacity retention rate of >85% (Figure 5(a)). Under the same conditions, the capacity of the Si@C negative electrode without fluorination treatment rapidly decayed during the charge and discharge process, and the capacity retention rate after 100 cycles was only 62%. It shows that the fluorine-doped carbon coating layer has a significant effect on improving the cycle stability of the silicon anode. Commercial nano-silicon anodes without carbon coating will fail after more than 10 cycles due to huge volume expansion and structural powdering during the deintercalation of lithium. During this process, the specific capacity of Si@C-F and Si@C negative electrodes gradually increases in the first 10 to 20 cycles due to the activation effect. At a large current density of 0.2~5.0 A·g-1, the Si@C-F anode can maintain a high specific capacity of 1540~580 mAh·g-1, showing excellent capacity retention (Figure 5(b)). At a high current density of 5.0 A·g-1, its capacity retention rate is approximately 78% higher than that of Si@C. When the current density is further reduced to 0.2 A·g-1, the specific capacity can be restored to 1450 mAh·g-1, indicating that its structure is highly stable during high-rate lithium storage. After 200 charge-discharge cycles at a current density of 0.2 A·g-1, the Si@C-F anode can maintain a specific capacity of >75 %. Die Kapazitätserhaltungsrate der Si@C-Anode ohne Fluorierungsbehandlung beträgt nur 40 % (Abbildung 5(c)). Diese Anode zeigt auch eine bessere Lithiumspeicherleistung als das in der Literatur beschriebene Siliziumanodenmaterial (Tabelle 1).

Abb. 5 (a) Zyklenstabilität bei einer Stromdichte von 0,4 A·g-1 mit Anoden, die durch 4 Zyklen bei 0,2 A·g-1 aktiviert wurden vor dem Zyklieren, und (b) Ratenfähigkeit bei verschiedenen Stromdichten im Bereich von 0.2 bis 5.0 A·g−1 und (c) Kapazitätserhaltung bei einer Stromdichte von {{13} }.2 A·g-1 für die Lithiumspeicherung in Si@C- und Si@CF-Anoden
Tabelle 1: Vergleich der Si@CF-Anode mit der gemeldeten Si-basierten Anode hinsichtlich der elektrochemischen Leistung
|
Materialien |
Erstes CE |
Anfangskapazität/(mAh·g-1) |
Kapazitätserhaltung |
Ref. |
|
Si@CF |
65.9% |
2640 |
85 % (100 Zyklen) |
Diese Arbeit |
|
Nano-Si/TiN@ |
71% |
2716 |
59,4 % (110 Zyklen) |
[20] |
|
Si@C@RGO |
74.5% |
1474 |
48,9 % (40 Zyklen) |
[21] |
|
Si@FA |
65% |
1334 |
68,7 % (100 Zyklen) |
[22] |
|
p-Si@C |
58% |
3460 |
57,5 % (100 Zyklen) |
[23] |
|
Si@void@C |
- |
900 |
70 % (100 Zyklen) |
[24] |
|
Si/C@C |
- |
1120 |
80 % (100 Zyklen) |
[25] |
At a high current density of 5.0 A·g-1, its capacity retention rate is approximately 78% higher than that of Si@C. When the current density is further reduced to 0.2 A·g-1, the specific capacity can be restored to 1450 mAh·g-1, indicating that its structure is highly stable during high-rate lithium storage. After 200 charge-discharge cycles at a current density of 0.2 A·g-1, the Si@C-F anode can maintain a specific capacity of >75%. The capacity retention rate of the Si@C anode without fluorination treatment is only 40% (Figure 5(c)). This anode also shows better lithium storage performance than the silicon anode material reported in the literature (Table 1). The fluorine doping amount in the coating carbon layer has a significant impact on the lithium storage performance of the Si@C-F anode. When the fluorine doping amount is below 1.8% atomic fraction, the cycling stability of the Si@C-F anode significantly improves as the fluorine doping amount increases (Figure 6). This is due to the enhanced effect of fluorine doping on the lithium ion transport properties of the carbon coating layer and the stability of the SEI film on the surface of the silicon material. When the fluorine doping ratio is too high (>2,7 % beträgt, behält das kohlenstoffbeschichtete Si-Anodenmaterial immer noch eine gute Zyklenstabilität bei, allerdings sinkt die spezifische Kapazität deutlich. Dies ist auf den Verlust an aktivem Si zurückzuführen, der durch das Ätzen von Fluorspezies in der Gasphase während der Hochtemperaturfluorierung verursacht wird. Bei einer Fluordotierungsmenge von 1,8 Atomprozent weist die Si@CF-Anode eine optimale Zyklenstabilität und eine hohe spezifische Kapazität auf.
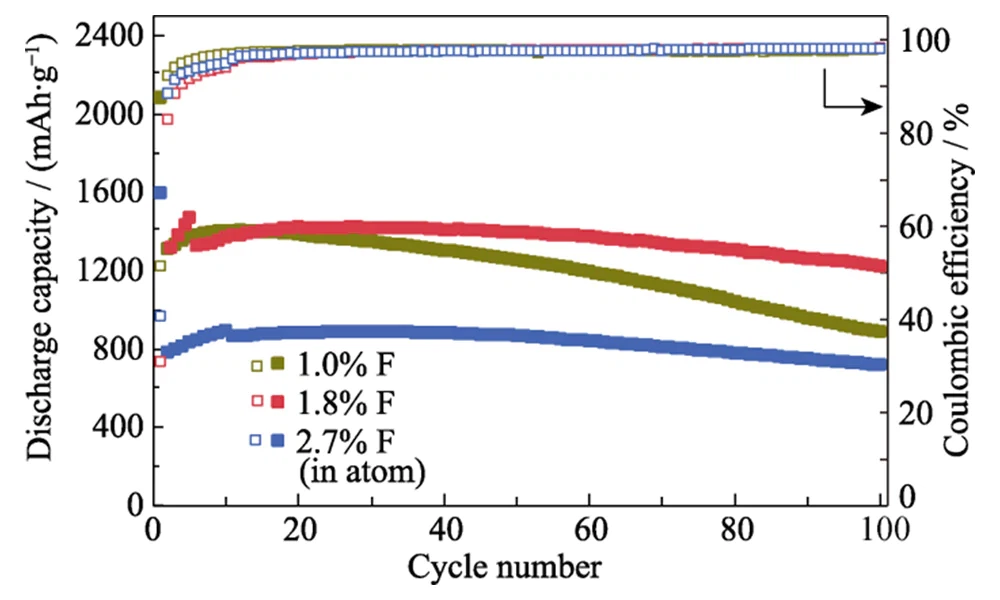
Abb. 6 Zyklenstabilität von Si@CF-Anoden mit unterschiedlichen F-Verhältnissen bei einer Stromdichte von 0,4 A·g-1 mit Anoden, die durch 4-10 Zyklen bei 0 aktiviert wurden .2 A·g-1 vor dem Radfahren
Die EIS-Spektren von Si@C- und Si@CF-Anoden bestehen aus Halbbogenkurven im Mittel- bis Hochfrequenzbereich und geneigten Geraden im Niederfrequenzbereich (Abbildung 7(a)). Die Halbbogenkurve im Mittel- bis Hochfrequenzbereich hängt mit dem Ladungsübertragungswiderstand (Rct) zusammen, und die geneigte Gerade im Niederfrequenzbereich spiegelt hauptsächlich die Warburg-Impedanz (ZW) der Lithiumionendiffusion wider [26 ]. Vor dem Laden und Entladen sind die Rct der negativen Si@CF- und Si@C-Elektroden ähnlich, erstere weist jedoch aufgrund der stark defekten, mit Fluor dotierten Kohlenstoffschicht, die die Oberfläche bedeckt, ein niedrigeres ZW auf. Nach Lade- und Entladezyklen ist der Rct (5,51 Ω) der Si@CF-Anode deutlich niedriger als der der Si@C-Anode (21,97 Ω) (Abbildung 7(b)), und der ZW ist viel niedriger als letzterer . Dies zeigt, dass der durch die fluordotierte Kohlenstoffschicht induzierte fluorreiche SEI-Grenzflächenfilm die Grenzflächenladung und die Lithiumionentransportfähigkeiten wirksam verbessern kann.
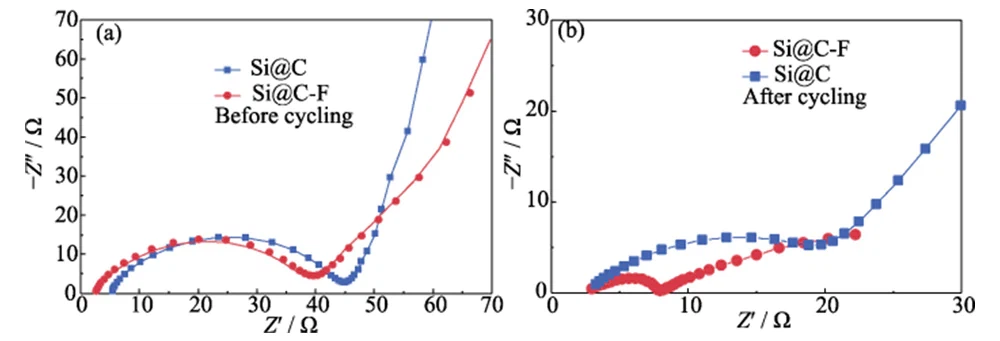
Abb. 7 Nyquist-Diagramme der Si@C- und Si@CF-Anoden (a) vor und (b) nach dem Zyklieren bei einer Stromdichte von 0.4 A·g-1
2.3 Charakterisierung der Elektrodenstruktur nach Ladung und Entladung
Die SEM-Charakterisierung nach Lade- und Entladezyklen (Abbildung 8(a~c)) zeigt, dass aufgrund des erheblichen Volumenausdehnungseffekts von Silizium während des Lithium-Einfügungsprozesses die Dicke der Si@C-Elektrode um 132,3 % zunahm. Dies behindert nicht nur die Übertragung von Ionen und Elektronen, erhöht den Innenwiderstand und die Polarisation der Elektrode, sondern verursacht auch enorme mechanische Spannungen, die dazu führen, dass die Elektrode reißt und sich vom Stromkollektor trennt, wodurch die Leistung der Si@C-Anode beeinträchtigt wird schnell zerfallen (Abbildung 5(c)). Im Vergleich dazu erhöhte sich die Elektrodendicke der Si@CF-Anode nach Lade- und Entladezyklen nur um 26,6 % und behielt eine gute strukturelle Stabilität der Elektrode bei (Abbildung 8(d~f)). Dies zeigt, dass die eingeführte fluordotierte Kohlenstoffschicht den Volumenexpansionseffekt der Lithiumeinfügung in Siliziummaterialien auf der Mikroskala wirksam abfedern kann, wodurch die strukturelle Stabilität der Elektrode auf der Makroskala von unten nach oben verbessert wird.

Abb. 8 Obere SEM-Bilder von (a) Si@C- und (d) Si@CF-Anoden nach dem Zyklieren; Querschnitt-REM-Bilder von (b, c) Si@C- und (e, f) Si@CF-Anoden (b, e) vor und (c, f) nach dem Zyklus; Hochauflösende (g) F1s- und (h) Li1s-XPS-Spektren von SEI auf Si@C- und Si@CF-Anoden nach dem Zyklus
Die Zusammensetzung des SEI-Films auf der Oberfläche von Si@C- und Si@CF-Negativelektroden nach Lade- und Entladezyklen wurde mittels XPS analysiert (Abbildung 8(g~h)). Im hochauflösenden F1s-XPS-Spektrum entsprechen die Bindungsenergiepeaks bei den Bindungsenergien 684,8, 688,3 und 689,1 eV LiF-, CF-Bindungen bzw. CF2. Dementsprechend gibt es auch charakteristische Peaks, die LiF-Spezies im hochauflösenden Li1s-XPS-Spektrum entsprechen, was darauf hindeutet, dass sich auf der Oberfläche der Siliziumanode ein SEI-Film gebildet hat, der LiF-Spezies enthält. Im Vergleich zur Si@C-Anode ist der LiF-Gehalt auf der Oberfläche der Si@CF-Anode höher, was darauf hindeutet, dass das LiF im SEI-Film nicht nur aus der Zersetzung von Lithiumsalzen im Elektrolyten, sondern auch aus dem darin enthaltenen F stammt die fluordotierte Kohlenstoffschicht. Die Bildung von hochmoduligem LiF kann die strukturelle Festigkeit des SEI-Films wirksam erhöhen und die Volumenänderung der Lithiumeinfügung in Siliziummaterialien hemmen. Gleichzeitig können die große Bandlücke und die isolierenden Eigenschaften von LiF die SEI-Dicke verringern und den anfänglichen irreversiblen Lithiumverlust verringern. Die LixSi-Legierung, das Lithiierungsprodukt von LiF und Si, weist eine hohe Grenzflächenenergie auf und kann sich während des Zyklierens besser an die plastische Verformung der lithiierten Siliziumanode anpassen, wodurch die Zyklenstabilität der Elektrode weiter verbessert wird [19].
3 Fazit
In this study, fluorine-doped carbon-coated nano-silicon materials were prepared through a simple and low-toxic gas-phase fluorination method. Research shows that fluorine doping (1.8% F), on the one hand, increases the defects of the carbon coating layer on the silicon surface, and provides abundant lithium ion transport channels while tightly coating nano-silicon to suppress its volume expansion. On the other hand, a highly stable SEI film rich in LiF is induced on the surface of the nano-silicon material, further improving the stability and Coulombic efficiency of the silicon anode. Thanks to this, the first Coulombic efficiency of the fluorine-doped carbon-coated nano-silicon anode improved to 65.9%. At a current density of 0.2~5.0 A·g-1, it exhibits a high specific capacity of 1540~580 mAh·g-1, and can maintain >75 % der ursprünglichen Kapazität nach 200 Zyklen. Diese Arbeit liefert neue Ideen für das Design und die Konstruktion von Siliziumanodenmaterialien mit hoher Kapazität und hoher Stabilität.
Referenz
[1] NIU SS, WANG ZY, YU ML, et al. MXen-basierte Elektrode mit verbesserter Pseudokapazität und volumetrischer Kapazität für leistungsstarke und extrem langlebige Lithiumspeicherung. ACS Nano, 2018, 12(4): 3928.
[2] SU
[3] GE MZ, CAO CY, GILL MB, et al. Jüngste Fortschritte bei siliziumbasierten Elektroden: von der Grundlagenforschung bis hin zu praktischen Anwendungen. Advanced Materials, 2021, 33(16): 2004577.
[4] LIP, ZHAO GQ, ZHENG
[5] LIU XH, ZHONG L, HUANG S, et al. Größenabhängiger Bruch von Siliziumnanopartikeln während der Lithiierung. ACS Nano, 2012, 6(2): 1522.
[6] LUO W, WANG YX, CHOU SL, et al. Kritische Dicke einer Kohlenstoffgrenzflächenschicht auf Phenolharzbasis zur Verbesserung der Langzeitstabilität von Silizium-Nanopartikelanoden. Nano Energy, 2016, 27: 255.
[7] DOU F, SHI LY, CHEN GR,Silizium/Kohlenstoff-Verbundanodenmaterialien für Lithium-Ionen-Batterien.Electrochemical Energy Reviews, 2019, 2(1): 149.
[8] JIA HP, ZOU LF, GAO PY, et al. Hochleistungs-Siliziumanoden, ermöglicht durch nicht brennbare lokalisierte hochkonzentrierte Elektrolyte. Advanced Energy Materials, 2019, 9(31): 1900784.
[9] CHOI SH, KWON TW, COSKUN A, et al. Hochelastische Bindemittel, die Polyrotaxane für Silizium-Mikropartikelanoden in Lithium-Ionen-Batterien integrieren. Wissenschaft, 2017, 357: 279.
[10] LI ZH, ZHANG YP, LIU TF, et al.Siliziumanode mit hoher anfänglicher Coulomb-Effizienz durch moduliertes trifunktionales Bindemittel für Lithiumionenbatterien mit hoher Flächenkapazität.Advanced Energy Materials, 2020, 10(20): 1903110.
[11] XU ZL, CAO K, ABOUALI S, et al. Untersuchung der Lithiierungsmechanismen von kohlenstoffbeschichteten Hochleistungs-Si-Anoden durch In-situ-Mikroskopie. Energy Storage Materials, 2016, 3: 45.
[12] TEKI R, MONI KD, RAHUL K, et al. Nanostrukturierte Siliziumanoden für wiederaufladbare Lithium-Ionen-Batterien. Small, 2009, 5(20): 2236.
[13] XIA SX, ZHANG
[14] ZHANG SL, WANG
[15] HUANG W, WANG Y, LUO GH, et al. 99,9 % Reinheit mehrwandiger Kohlenstoff-Nanoröhrchen durch Vakuum-Hochtemperatur-Glühen. Carbon, 2003, 41(13): 2585.
[16] MCDOWELL MT, LEE SW, NIX WD, et al. Artikel zum 25-jährigen Jubiläum: Verständnis der Lithiierung von Silizium und anderen Legierungsanoden für Lithium-Ionen-Batterien. Advanced Materials, 2013, 25(36): 4966.
[17] KEY B, MORCRETTE M, TARASCON J M. Paarverteilungsfunktionsanalyse und Festkörper-NMR-Untersuchungen von Siliziumelektroden für Lithium-Ionen-Batterien: Verständnis der (De)Lithiierungsmechanismen. Journal of American Chemical Society, 2011, 133(3) : 503.
[18] GAO H, XIAO LS, PLUMEL I, et al. Parasitäre Reaktionen in nanoskaligen Siliziumanoden für Lithium-Ionen-Batterien. Nano Letters, 2017, 17(3): 1512.
[19] CHEN J, FAN XL, LI Q, et al.Elektrolytdesign für LiF-reiche Festelektrolyt-Schnittstellen zur Ermöglichung hochleistungsfähiger Mikrolegierungsanoden für Batterien.Nature Energy, 2020, 5(5): 386.
[20] ZHANG P, GAO YQ, RU Q, et al.Skalierbare Herstellung einer porösen Nano-Silizium/TiN@Kohlenstoff-Anode für Lithium-Ionen-Batterien.Applied Surface Science, 2019, 498: 143829.
[21] SU MR, WAN HF, LIU YJ, et al.Mehrschichtiger kohlenstoffbeschichteter Si-basierter Verbundwerkstoff als Anode für Lithium-Ionen-Batterien.Powder Technology, 2018, 323: 294.
[22] PU JB, QIN J, WANG YZ, et al.Synthese eines Silizium-Kohlenstoff-Verbundwerkstoffs mit Mikro-Nano-Kugelstruktur als Anodenmaterial für Lithium-Ionen-Batterien.Chemical Physics Letters, 2022, 806: 140006.
[23] GAO RS, TANG J, YU XL, et al. Ein sandwichartiger Silizium-Kohlenstoff-Verbundstoff, hergestellt durch Oberflächenpolymerisation für die schnelle Lithium-Ionen-Speicherung.
Nanoenergie, 2020, 70: 104444.
[24] GONG
[25] LIA YR, WANG RY, ZHANG JW, et al.Sandwichstruktur kohlenstoffbeschichteter Silizium-/Kohlenstoff-Nanofaseranoden für Lithium-Ionen-Batterien.Ceramics International, 2019, 45: 16195.
[26] YANG XM UND ROGACH A L. Elektrochemische Techniken in der Batterieforschung: ein Tutorial für Nicht-Elektrochemiker. Advanced Energy Materials, 2019, 9(25): 1900747.





